 Formação de ligações covalentes, em que os átomos compartilham partículas como os elétrons, é um dos principais meios de coesão envolvidos no surgimento de moléculas, biomoléculas (DNA e proteínas, por exemplo), e também de alguns sólidos – Foto: p_a_h/Flickr
Formação de ligações covalentes, em que os átomos compartilham partículas como os elétrons, é um dos principais meios de coesão envolvidos no surgimento de moléculas, biomoléculas (DNA e proteínas, por exemplo), e também de alguns sólidos – Foto: p_a_h/Flickr
.
…
Simulações realizadas em computador apontam uma nova maneira dos átomos, unidades básicas dos elementos químicos, se unirem para formarem moléculas, conclui pesquisa com participação do Instituto de Física (IF) da USP. No processo habitual, os átomos compartilham elétrons para ganhar estabilidade e formar moléculas, o que é chamado de ligação covalente eletrônica. No estudo, a ligação foi conseguida com a adição de uma partícula de antimatéria chamada pósitron, semelhante ao elétron, mas com carga elétrica oposta. Por não envolver elétrons, o fenômeno foi denominado ligação covalente não eletrônica, ou positrônica.
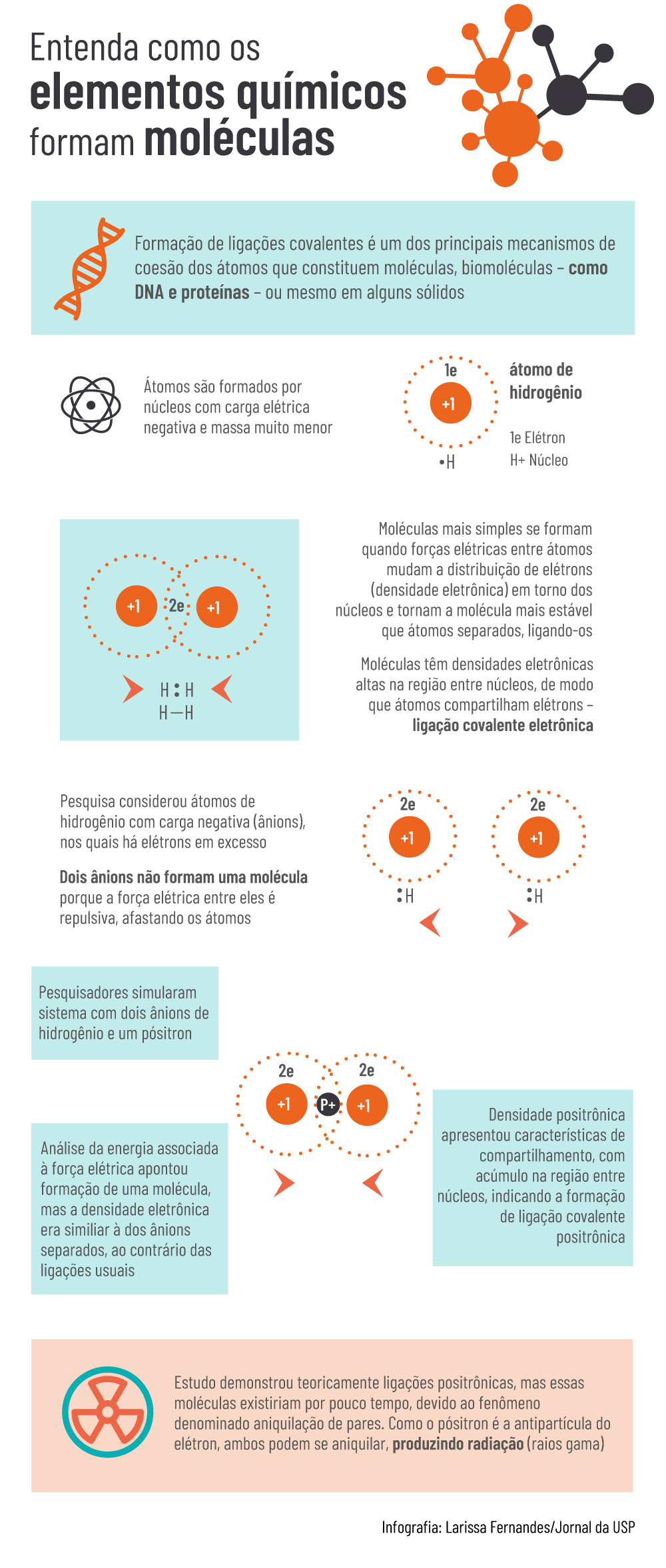
A formação de ligações covalentes é um dos principais mecanismos de coesão dos átomos que constituem moléculas, biomoléculas (como DNA e proteínas) ou mesmo em alguns sólidos. “Os átomos são formados por núcleos com carga elétrica positiva, e elétrons com carga elétrica negativa e massa muito menor”, afirma o físico Márcio Teixeira do Nascimento Varella, professor do IF, que participou da pesquisa.

As moléculas mais simples são constituídas por apenas dois átomos, e se formam quando as forças elétricas entre os átomos modificam a concentração de elétrons (densidade eletrônica) em torno dos núcleos. “Esse processo torna a molécula mais estável que os dois átomos separados, ligando-os”, relata Varella. “As moléculas apresentam densidades eletrônicas altas na região entre os núcleos atômicos de forma que os átomos compartilham elétrons, caracterizando a formação de uma ligação covalente eletrônica.”
Na pesquisa, foram considerados átomos de hidrogênio com carga negativa, denominados ânions, nos quais há elétrons em excesso. “Dois ânions não formam uma molécula”, diz o físico, “porque a força elétrica entre eles é repulsiva, afastando os átomos”. Os pesquisadores simularam no computador o sistema formado por dois ânions de hidrogênio e um pósitron.
Energia
“A análise da energia associada à força elétrica apontou claramente a formação de uma molécula, mas a densidade eletrônica era muito semelhante à densidade dos ânions separados, ao contrário do que acontece na formação de ligações covalentes usuais”, explica o professor. “Por outro lado, a densidade positrônica apresentou características de compartilhamento, com acúmulo na região entre os núcleos, o que levou à conclusão sobre a formação de uma ligação covalente positrônica.”
…
“O estudo demonstrou teoricamente a existência de ligações positrônicas, mas as moléculas assim formadas existiriam por curtos períodos de tempo, em consequência de um fenômeno denominado aniquilação de pares”, afirma o pesquisador. “Como o pósitron é a antipartícula do elétron, ambos podem se aniquilar, produzindo radiação (raios gama).”
Segundo o professor Varella, dezenas de moléculas positrônicas já foram produzidas em laboratório, por meio de colisões entre pósitrons e moléculas comuns. “Nesse caso, moléculas estáveis capturam o pósitron, sem formação de ligações. Essa técnica não pode ser utilizada para induzir a formação de ligações positrônicas, pois os ânions não formam uma molécula estável”. O físico acredita que métodos experimentais alternativos permitiriam produzir moléculas estabilizadas por ligações positrônicas. “Foram propostos experimentos, ainda não realizados, para produzir átomos positrônicos, que poderiam reagir com ânions e formar ligações positrônicas.”
A pesquisa é descrita no artigo Binding Matter with Antimatter: The Covalent Positron Bond, de autoria de Jorge Charry, Varella e do professor Andrés Reyes, publicado na revista científica Angewandte Chemie International Edition. Charry e Reyes são pesquisadores da área de química na Universidade Nacional de Colômbia, em Bogotá.
Mais informações: e-mail mvarella@if.usp.br, com o professor Márcio Teixeira do Nascimento Varella



