Caminante no hay camino, se hace camino al andar
Antonio Machado Ruiz
Esta viagem só cabe neste artigo fazendo saltos na história, deixando de mencionar muitos cientistas que, como eu, caminharam para construir este caminho.
Plínio, o Velho, na sua vasta enciclopédia, descreve de que modo a adição de óleo acalma as rugosidades da água. Esta observação documentada provava que óleo e água não se misturam e que a tensão interfacial modificava as propriedades de uma solução salina. Esse naturalista é descrito, no primeiro século da nossa era, logo após sua trágica morte, pelo seu sobrinho Plínio, o Jovem:
“Felizes, eu estimo, aqueles a quem, por provisão dos deuses, foi concedida a capacidade de fazer tais ações que são dignas de serem relatadas ou relacioná-las de uma maneira digna de ser lida; mas particularmente felizes são aqueles que são abençoados com esses dois talentos incomuns: no número dos quais meu tio, como seus próprios escritos e sua história evidentemente provarão, pode ser classificado com justiça”.
Sem crer em deuses, esta descrição pode se aplicar a muitos dos cientistas que conseguiram, nestes dois milênios, transformar a observação do Plínio, o Velho, em uma poderosa ferramenta de transporte de drogas e vacinas. Uma série de filósofos naturais e cientistas, nos séculos subsequentes, descreveram propriedades de corpos d’água recobertos com uma série de substâncias oleosas.
Os caminhantes aceleram a construção de caminhos a partir do século 20. Katharine Burr Blodgett e Irving Langmuir descrevem, nas primeiras décadas desse século, as propriedades de uma única camada de moléculas, quando uma superfície de água é coberta por óleo. Esta descoberta, de um teor físico-químico, foi a pedra fundamental que permitiu a descoberta da composição, bem como as primeiras propostas da estrutura, das membranas biológicas. A relação entre as propriedades de uma camada de óleo e as membranas biológicas foi possível graças a uma nova tecnologia (a balança de Langmuir-Blodgett) e a engenhosidade de dois cientistas de um departamento de pediatria na Holanda, em 1925. Gorter e Grendel extraíram substâncias gordurosas de células do sangue humano, de coelhos e ovelhas e, espalhando essas substâncias em uma balança de Langmuir-Blodgett, medem a área ocupada por esses materiais e propõem que as células estavam delimitadas por uma dupla camada de substâncias que denominaram lipoides.
A estrutura dos componentes dos “lipoides” era, na época uma enorme confusão. Em uma conferência organizada em 1927 se concluiu que:
“Quando consideramos a obscuridade em que a química dos fosfolipídios foi envolta, é fácil entender que muitas das propriedades e funções atribuídas a esses corpos são baseadas em pouco mais do que imaginação”.
O progresso de técnicas como a cromatografia em papel e em sílica, bem como o desenvolvimento de tecnologias de separação e análise, permitiu, na década seguinte, a definição da estrutura química dos componentes majoritários das membranas biológicas, os fosfolipídios e o colesterol.
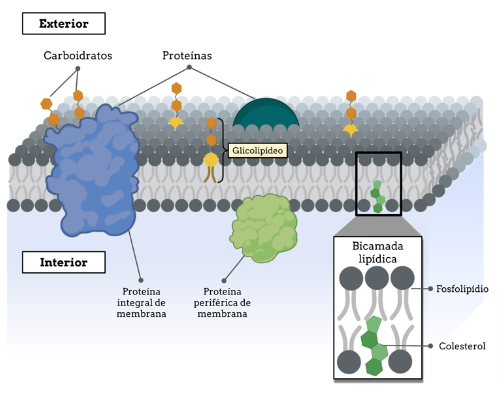
A composição lipídica e um modelo de membranas, graças às contribuições de Danielli e Davson em 1937, asseguravam o avanço da nossa compreensão das estruturas que delimitam as células e muitas das estruturas intracelulares. Um modelo que até agora descreve com mais detalhe e apresenta condições de explicação de uma série de dados experimentais é o chamado mosaico fluido, proposto por Singer e Nicholson em 1972. Uma representação pictórica deste modelo é mostrada na figura a seguir. Hoje, apesar da sua popularidade, este modelo é sujeito a uma série de restrições.
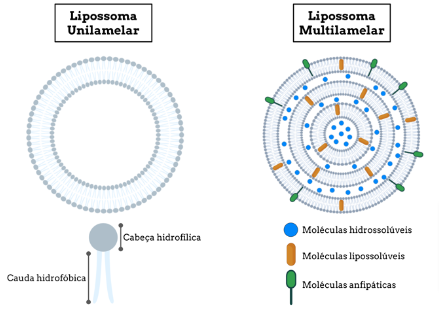
O intenso interesse pelas membranas biológicas trouxe à luz, também, a complexidade dessas estruturas. Decorrentes desta complexidade, sistemas mais simples foram elaborados para compreender com algum detalhe fenômenos específicos sem toda a complexidade da membrana. Dentre estes, cito as palavras de A. D. Bangham que, no começo da década de 1960, observando dispersões de fosfolipídios extraídos de lecitina de ovo, escreveu: “Brinquei com manchas de lecitina em lâminas de microscópio e fiquei fascinado com a forma como reagiram com a água para formar estruturas móveis de delicada e complexa estrutura”. Bangham, na época interessado pelo papel dos lipídios na coagulação, se deu conta que tinha nas mãos um dos mais poderosos sistemas-modelo de membranas biológicas, os lipossomos. A primeira microfotografia eletrônica dessas estruturas, publicada por ele em 1964, mostrava uma verdadeira cebola, onde cada casca esférica era composta de uma camada dupla, composta de fosfolipídios que, separada por uma região aquosa, continha uma esfera menor da mesma composição, como mostra a figura abaixo:
As profundas implicações da formação espontânea de estruturas fechadas que separam um compartimento aquoso interno do meio que as rodeia já começaram a ser conjeturadas a partir dessa época. Escolas de pensamento sobre a origem da vida descansam sobre a hipótese de que vida pode aparecer em uma estrutura primordial, como um lipossomo. Nestes agregados espontâneos fenômenos autopoiéticos, na concepção do Humberto Matura [A árvore do Conhecimento, ISBN-10-857242032], de autopreservação da estrutura seriam possíveis. Um lipossomo, embora fechado, permite a comunicação com o meio externo pela difusão de algumas moléculas através da membrana.
Noutro caminhar, vislumbrando já outro caminho, destaco um cientista grego, formado primeiro na Grécia e depois na Inglaterra e nos Estados Unidos, Gregory Gregoriadis. Gregory é um humanista, autor de um romance sobre a adolescência na Grécia ocupada pelos nazistas, cientista de imensa criatividade e CEO de empresas de biotecnologia. O jovem cientista/poeta grego, de volta dos Estados Unidos onde obteve o PhD, começa um pós-doutorado em Londres. O primeiro trabalho desse estágio é premonitório e, em tradução livre o transcrevo, pois o caminhar deste jovem grego em 1971 parece desenhar outro caminho – Lipossomas como transportadores de enzimas ou drogas: uma nova abordagem para o tratamento de doenças de armazenamento. Este trabalho provocou uma febre de interesse, e publicações, pelo uso de lipossomos como transportadores de drogas, e na mesma época são descritas moléculas sintéticas que formam vesículas unilamelares e lipossomos.
O entusiasmo da comunidade científica interessada em usar lipossomos como carregadores universais de drogas durou pouco, pois resultados posteriores demonstraram que, in vivo, quando injetados, os lipossomos são eliminados de forma eficiente por células circulantes.
Como toda história longa, o interesse em utilizar lipossomos como carregadores de drogas recebeu um novo impulso quando Alexander Klibanov descreve que a adição de cadeias de um polímero de etilenoglicol à membrana do lipossomo evitava a destruição rápida destes carregadores. E assim, já em 1995 a Administração Federal de Alimentos e Medicamentos (FDA) dos Estados Unidos aprova a primeira droga (Doxil) injetável contra o câncer veiculada em lipossomos.
Gregoriadis, no seu encantamento com a ideia formulada na década de 1970, continua a contribuir e já no início deste século descreve uma vacina de DNA encapsulada em lipossomos.
Os caminhantes já podiam vislumbrar este caminho. Era claro, então, que a modificação da composição da membrana do lipossomo que levasse ao aumento da vida deste carregador no sangue do paciente, bem como a estabilidade do material do compartimento interno, eram requisitos para usá-lo na prática clínica.
Como tentei demonstrar, o caminhar de muitos cientistas construiu o caminho que permitiu vacinar milhões de pessoas contra as formas mais graves de covid, contribuindo assim para que hoje possamos vislumbrar o fim da pandemia. Dois cientistas, cujas descobertas levaram ao uso de vacinas de RNA mensageiro (mRNA), são a Katalin Karikó e o Ian Maclachlan. Katalin Karikó dedicou boa parte da sua carreira como cientista ao estudo do mRNA. O seu percurso merece um artigo separado, porque a carreira acadêmica e as dificuldades que ela enfrentou para fazer pesquisa em um ambiente conservador que não apreciava as suas descobertas são exemplos que, depois de superar muitas barreiras, a levaram a descobertas que permitiram o uso de um mRNA estável dentro de um lipossomo. A composição do lipossomo é a parte da história que, em um mercado de bilhões de dólares, está até hoje em disputas de patentes. Poucas dúvidas me restam de que Ian Maclachlan é um dos cientistas que formulou, pela primeira vez, uma composição lipossomal que, no fim e junto com o mRNA estável, levou à vacina contra a covid da Moderna e da Pfizer.
E assim chegamos ao fim de uma viagem, que já dura mais de dois milênios, por um caminho que não termina, pois os cientistas caminhantes, na sua curiosidade, podem nos trazer descobertas que nem podemos imaginar e, com isso, abrir novos e incríveis caminhos.
P.S.: Um agradecimento especial para Danilo Kiyoshi Matsubara, autor das ilustrações deste texto.