Blog
Molécula inédita que poderia inibir a progressão de leucemia passa por testes
Em fase de experimentos no laboratório, novo composto foi capaz de eliminar células cancerosas e impedir sua multiplicação em mais de 20 modelos celulares de cânceres do sangue
Pesquisadores do Instituto de Ciências Biomédicas (ICB) da USP testaram uma nova molécula capaz de inibir a progressão do ciclo celular da leucemia — câncer sanguíneo causado pela reprodução descontrolada dos glóbulos brancos na medula óssea. O estudo, publicado na revista Toxicology in Vitro, mostrou que o novo composto foi eficaz em combater as células leucêmicas sem apresentar toxicidade nas saudáveis.
Inédita, a molécula C2E1 foi sintetizada pelo grupo de pesquisa liderado pelo cientista Fernando Coelho, professor do Instituto de Química da Universidade Estadual de Campinas (IQ-Unicamp), e funciona como inibidora da tubulina, uma proteína que constitui os microtúbulos. Componentes do citoesqueleto celular, essas estruturas têm um papel fundamental no processo de mitose — divisão em que são formadas duas células a partir de uma —, pois atuam na distribuição do material genético entre a célula “original” e a que está sendo formada. Dessa forma, ao inibir a tubulina, o composto interrompe a multiplicação das células cancerosas, impedindo o avanço da leucemia.
“O meu trabalho já envolvia o estudo dos esqueletos dos microtúbulos como alvo farmacológico para leucemia. Quando recebemos esse composto do professor Coelho, que sugeriu uma possível interação com a tubulina, resolvemos elucidar esse mecanismo e entender seus efeitos celulares e moleculares”, conta o doutorando Hugo Passos Vicari, primeiro autor do estudo. Os testes, realizados in vitro (em laboratório), com células cultivadas fora de organismos vivos, mostraram que a molécula foi eficaz em eliminar as células cancerosas e impedir sua proliferação em 21 dos 25 modelos celulares testados. Além disso, o estudo confirmou a não-toxicidade em células saudáveis do sangue, o que sugere um potencial para menos efeitos colaterais em um possível fármaco no futuro.
Segundo Vicari, o estudo envolveu diferentes testes, expondo células de leucemia aos compostos. “A princípio, verificamos se o composto apresentava o efeito tóxico capaz de matar as células, chamado de citotoxicidade. Depois, observamos se ocorreu de fato a morte celular. Por último, constatamos se houve interrupção no ciclo de divisão celular, processo que chamamos de catástrofe mitótica”, relata. Foram testados diversos modelos celulares com características distintas. Nesse sentido, pôde-se observar a efetividade do composto em diversas variações da doença, da leucemia linfoblástica aguda, mais comum em crianças e jovens adultos, à leucemia mieloide aguda, mais comum em adultos a partir dos 60 anos. Medicamentos são ainda mais importantes para essa última faixa etária, inelegível para transplante de medula óssea, a única cura para a leucemia.

Teixo-do-pacífico, árvore nativa da costa oeste da América do Norte, matéria-prima de um dos medicamentos usados no tratamento da leucemia -Foto: Reprodução do artigo/ICB-USP
Terapias combinadas
Compostos que têm como alvo a tubulina já são usados no tratamento de diversas formas de câncer desde os anos 1940. Apesar do histórico de sucesso, a busca por alternativas é constante, uma vez que a adequação a cada medicamento pode variar de acordo com o paciente. “Ainda que a tubulina seja um bom alvo, com efetividade comprovada, os fármacos disponíveis nem sempre garantem uma terapia completa: é comum que pacientes desenvolvam resistência aos medicamentos meses ou até anos depois, como em casos em que um tumor retorna”, explica João Agostinho Machado-Neto, professor do Departamento de Farmacologia do ICB e coordenador do estudo. “Por isso, terapias combinando mais de uma opção são interessantes: quando o paciente adquire resistência a um composto, inicia-se o tratamento com outro”, acrescenta.
Nesse contexto, a nova molécula testada se mostrou uma opção eficaz, já que os pesquisadores verificaram sua efetividade em modelos celulares que já eram resistentes aos inibidores conhecidos. “O local de ligação do C2E1 na tubulina é diferente de outros, como o dos medicamentos Vincristina e do Paclitaxel, por exemplo. Por se ligar a um sítio diferente, o novo composto não apresenta a mesma resistência que os anteriores”, explica Vicari.
O Instituto Nacional do Câncer (Inca), responsável pelas estatísticas sobre câncer no Brasil, estima cerca de 11 mil pacientes que poderiam se beneficiar de novos tratamentos, sobretudo em casos de recaída. “Existem muitos tratamentos que são ótimos, mas tratam de tipos específicos de leucemia. Nosso tratamento poderia ser aplicado em contextos em que outros não cabem”, aponta Machado-Neto.
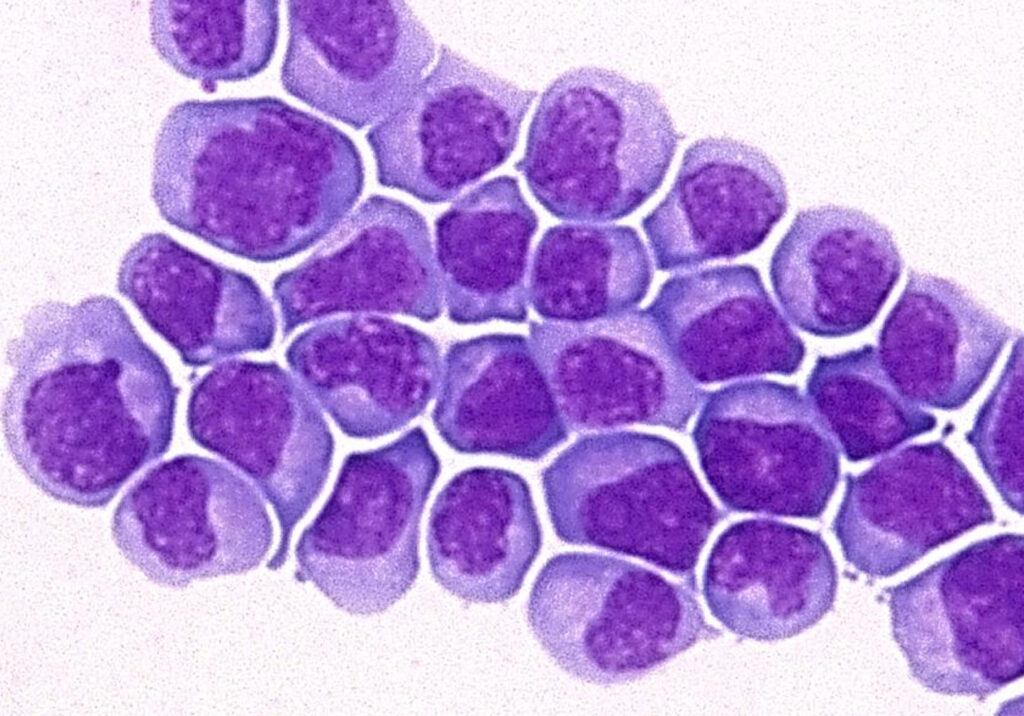
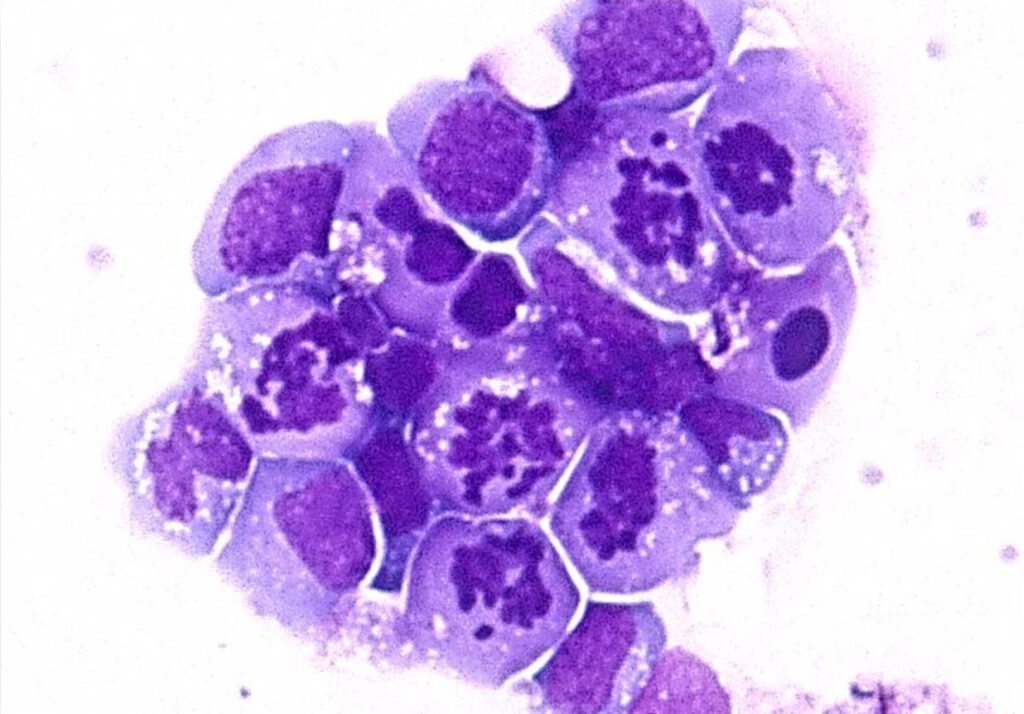
Células leucêmicas
Células leucêmicas tratadas com C2E1 (à direita) e do grupo controle (à esquerda); as células tratadas com o novo composto apresentam cromossomos condensados (estruturas que contêm o DNA e são fundamentais para divisão correta do material genético) e mitoses aberrantes nas células de leucemia - Imagens: Reprodução do artigo
Outra vantagem do novo inibidor é o fato de ele ser de fácil síntese em laboratório. O mesmo não vale para os já citados componentes da Vincristina, extraídos das vincas, e do Paclitaxel, extraídos do teixo-do-pacífico, árvore conhecida por seu crescimento lento. Quando foram descobertos, esses compostos só podiam ser obtidos por meio de suas plantas de origem, processo lento e trabalhoso. “Para se obter a quantidade necessária de Paclitaxel, como parte do primeiro ensaio clínico com o composto na época, foram derrubadas milhares de árvores centenárias”, conta Machado-Neto. Hoje ambas as substâncias já podem ser semi-sintetizadas por cientistas, processo que, apesar de mais rápido, ainda depende parcialmente das plantas de origem, ao contrário da C2E1, 100% sintetizável em laboratório.
Segundo a dupla, o próximo passo do trabalho seria o teste em modelos animais para verificar se os resultados se mantêm em sistemas mais complexos ou apresentam toxicidade em órgãos não previstos. Essa etapa levará de dois a cinco anos. Só então a molécula será avaliada em ensaios clínicos, que levam em média mais dois ou três anos. “Além da leucemia, temos interesse em investigar outros tipos de câncer tratados com inibidores de microtúbulos, como os cânceres de mama e de cólon. Também estamos otimistas com a possibilidade de modificar o composto, aumentando sua potência e diminuindo as doses necessárias para os efeitos terapêuticos, bem como potenciais efeitos adversos”, diz Machado-Neto.
O trabalho tem apoio da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) e do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq).
Mais informações: e-mail comunicacao@icb.usp.br
*Do Núcleo de Comunicação do ICB, adaptado por Júlio Bernardes
**Estagiária supervisionada por Moisés Dorado
A reprodução de matérias e fotografias é livre mediante a citação do Jornal da USP e do autor. No caso dos arquivos de áudio, deverão constar dos créditos a Rádio USP e, em sendo explicitados, os autores. Para uso de arquivos de vídeo, esses créditos deverão mencionar a TV USP e, caso estejam explicitados, os autores. Fotos devem ser creditadas como USP Imagens e o nome do fotógrafo.